Tecnología de síntesis de péptidos
La investigación y el desarrollo de medicamentos peptídicos está creciendo rápidamente en medicina. Sin embargo, el desarrollo de fármacos peptídicos está limitado por sus propias características. Por ejemplo, debido a la sensibilidad especial a la hidrólisis enzimática, la estabilidad se reduce y la variabilidad de la conformación estérica da como resultado una baja especificidad de orientación, baja hidrofobicidad y falta de un sistema de transporte específico. Para superar estos péptidos, propuso muchas soluciones y la aplicación exitosa de un tipo de péptido es uno de ellos.
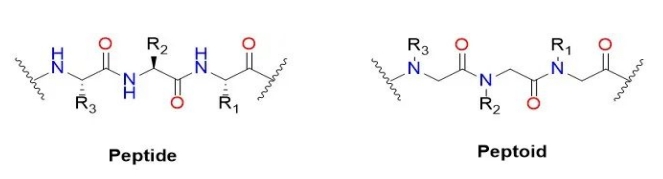
Tipo de péptido (nombre en inglés: peptoide) o poli - N - en lugar de glicina (nombre en inglés: poli real - n --glicina sustituida), es un compuestos cuasi péptidos de péptido en la cadena principal. La cadena lateral de carbono alfa transfiere el nitrógeno de la cadena principal en lugar de la cadena lateral. En el polipéptido original, el grupo R de la cadena lateral de aminoácidos representa 20 aminoácidos diferentes, pero el grupo R tiene más opciones en el peptoide. En el péptido, el péptido en la cadena principal de aminoácidos en el nitrógeno alfa carbono en lugar de la transferencia de la cadena lateral a la cadena principal. Vale la pena mencionar que los péptidos en general no producen las mismas estructuras ordenadas de alto nivel que las estructuras secundarias en péptidos y proteínas debido a la falta de hidrógeno en la columna vertebral de nitrógeno. El propósito inicial del péptido es desarrollar péptido estable y proteasa de fármacos de moléculas pequeñas.
Análisis de técnicas de síntesis de péptidos
Se introdujo el método de síntesis de péptidos
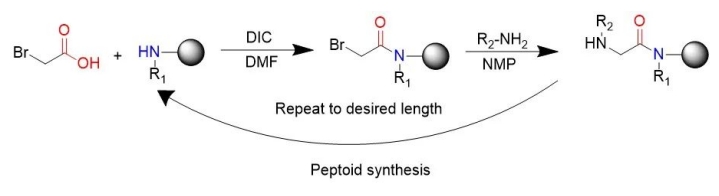
El método de síntesis de péptido generalmente popular es el método de síntesis de subsingle inventado por Ronzuckermann, cada uno de los cuales se divide en dos pasos: acilación y desplazamiento. En la acilación, el primer paso es activar el ácido haloacético para reaccionar con las aminas restantes al final del paso anterior, más comúnmente diisopropilo de diimina carbonizada. El bromoaceticácido se activó por diisopropilcarbodiimida. "En reacciones de sustitución (reacciones de sustitución nucleofílica bimolecular), una amina, típicamente primaria, ataca el halógeno alternativo para formar una glicina de N-sustituida por N". La ruta sintética subunitaria utiliza aminas primarias fácilmente disponibles para generar péptidos, lo que permite la síntesis química de péptidos.
La síntesis de la extensión sólida en los péptidos de clase tiene la rica experiencia, puede proporcionarle un tipo de tipo de servicio de síntesis de péptidos.
Análisis de técnicas de síntesis de péptidos
La ventaja de tal péptido
Más estable: los peptoides son más estables in vivo que los péptidos.
Más selectividad: los peptoides son muy adecuados para estudios combinados de descubrimiento de fármacos porque se puede obtener una gran variedad de diferentes bloques de construcción de polipéptidos mediante la modificación del grupo amino de la columna vertebral.
Más eficiente: la abundancia de estructuras peptroides puede hacer que el peptoide sea una buena opción para la metodología de escaneo para encontrar rápidamente estructuras específicas que se unan a las proteínas.
Más potencial de mercado: las características del tipo de péptido permiten que se convierta en un tipo de desarrollo de fármacos tiene un gran potencial.
Tiempo de publicación: 2025-07-02