¿Qué son los aminoácidos?
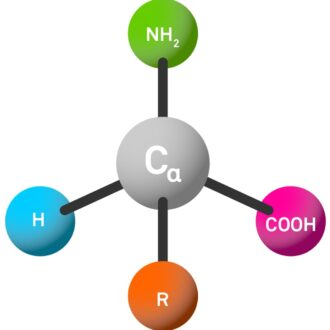
Los aminoácidos más comunes en la naturaleza se denominan α-aminoácidos. Estas moléculas tienen cuatro sustituyentes diferentes unidos al átomo de carbono central (llamado átomo de α-C):
Aminado (NH₂, código de tres letras abreviado como "H-").
Grupo de ácido carboxílico (COOH, abreviado como "-OH" en el código de tres letras).
Cadenas laterales(R, que son muy variables y determinan las propiedades de los aminoácidos, así como el péptido final).
Átomo de hidrógeno (H).
La conexión de los átomos de α-C con estos cuatro grupos diferentes le brinda propiedades químicas únicas, que juegan un papel clave en la determinación del comportamiento y las propiedades de los aminoácidos y los péptidos.
Actividad biológica de los aminoácidos
Los aminoácidos pueden exhibir actividades biológicas como:
El triptófano (TRP) y el ácido glutámico (Glu) juegan un papel clave en los procesos metabólicos.
El grupo R (o cadena lateral) determina las propiedades únicas de los aminoácidos. Estos grupos pueden:
En términos simples:Un átomo de hidrógeno como la glicina (Gly).
Se incluyen otros ácidos: como el ácido aspártico (ASP) y el ácido glutámico (Glu).
Llevar grupos básicos:Arginina (Arg), lisina (Lys) o histidina (His).
Contiene grupos polares: como serina (ser) o treonina (thr).
Hidrocarburos no polares:Alanina (ALA), fenilalanina (PHE) o valina (Val).
Contenido de azufre:Como se ve en cisteína (Cys) y metionina (MET).
El papel de los l-aminoácidos y los d-aminoácidos
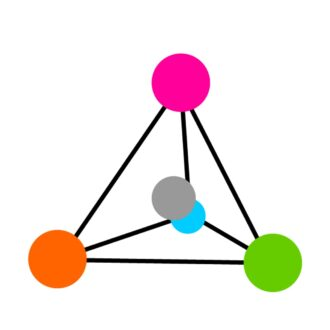
Los cuatro sustituyentes del átomo α-C están dispuestos en las esquinas del tetraedro, con el átomo α-C en el centro (ver Figura 3). Esta disposición permite que las dos formas de moléculas de aminoácidos existan en forma de espejo, similar a las manos izquierda y derecha. Estas formas de espejo se conocen como "estereoisómeros" o "enantiómeros".
Importancia biológica de los enantiómeros
Aunque los enantiómeros tienen propiedades químicas y físicas casi idénticas, sus efectos biológicos pueden diferir significativamente. La forma molecular es crítica para su interacción con objetivos biológicos. Un enantiómero puede unirse de manera efectiva al objetivo, otro puede no, o en algunos casos tener un efecto negativo. En solución, el enantiómero gira el plano de luz polarizado en la dirección opuesta.
Tiempo de publicación: 2025-09-05
